Un estudio coliderado por el Instituto de Neurociencias UMH-CSIC descifra las claves genómicas de la atrofia del hipocampo en la epilepsia
10 de junio de 2021
•El trabajo, coliderado por los Institutos Cajal de Madrid y Neurociencias de Alicante, identifica el mapa de transcripción genética de los tipos celulares implicados y proporciona claves para comprender mejor la epilepsia del lóbulo temporal.
•La inflamación provocada por las células inmunes del cerebro en una zona muy localizada del hipocampo está estrechamente asociada a la destrucción de algunas de las neuronas piramidales, fundamentales para la formación de la memoria.
•Analizando el perfil de expresión génica de las células han identificado genes que se expresan de manera muy específica en diferentes capas de la región CA1 del hipocampo. Esos genes podrían representar nuevas dianas terapéuticas o herramientas diagnósticas.
•Los resultados de este estudio podrían aplicarse también a patologías asociadas con el envejecimiento cerebral, como el Alzheimer.
Genes que se expresan de forma diferente en diferentes tipos celulares de una región del hipocampo denominada CA1, implicada en la formación de la memoria, son responsables de la atrofia o esclerosis asociada a la epilepsia del lóbulo temporal. Esta es la conclusión de un trabajo que se publica hoy en Cell Reports (“Trayectorias transcripcionales neurodegenerativas específicas para cada subcapa y tipo de célula en la esclerosis del hipocampo”). La investigación está coliderada por el Instituto Cajal del CSIC de Madrid y el Instituto de Neurociencias UMH-CSIC en Alicante.
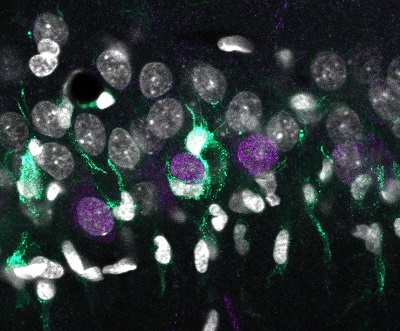
"Acumulación desigual de microglía (turquesa) alrededor de las neuronas superficiales de CA1 (en violeta), rodeados por otros núcleos celulares (blanco)".
Crédito: Elena Cid, Instituto Cajal.
El trabajo liderado por Liset Menéndez de la Prida, del Instituto Cajal del CSIC, y José López-Atalaya, del Instituto de Neurociencias UMH-CSIC, en Alicante, ha descubierto que esta atrofia se caracteriza por la muerte de una población de neuronas denominadas piramidales en la capa superficial de la región CA1 del hipocampo. Además, han comprobado que esa muerte celular está asociada a una hiperactivación exagerada de otros tipos celulares residentes en el cerebro, como la microglía (sistema inmune del cerebro) y los astrocitos (células que proporcionan soporte y avituallamiento a las neuronas y que también están implicadas en funciones clave, como el aprendizaje o la memoria).
Tanto la microglía (los macrófagos del cerebro) como los astrocitos se activan en situaciones patológicas, cambiando incluso su morfología, y pueden contribuir a la puesta en marcha de procesos de inflamación asociados a la muerte de las neuronas piramidales.
Hasta ahora se desconocía por qué algunos tipos neuronales son más vulnerables que otros. En este trabajo, los investigadores han desarrollado un mapa genómico que identifica el código genético preciso de todos los tipos celulares implicados en la enfermedad. “Los mapas genómicos intentan asignar diferentes genes con elementos biológicos concretos. En el caso del cerebro, se trata de vincular una serie de genes con tipos neuronales específicos, como las neuronas, los astrocitos y la microglía”, explica Liset Menéndez de la Prida.
“Hemos visto en modelos de epilepsia en rata y ratón que hay regiones en el hipocampo más vulnerables a la epilepsia desde el punto de vista de la neurodegeneración. Se sabe desde hace poco que la región CA1 del hipocampo tiene una estructura laminar, y hemos visto que la capa superficial tiene mayor vulnerabilidad y degenera antes”, detalla López-Atalaya.
Para llegar a estas conclusiones han llevado a cabo un detallado estudio que incluye análisis genómicos, histológicos y electrofisiológicos. Estos tres enfoques han permitido ver que la capa superficial de la región CA1 del hipocampo es más vulnerable y tiene más propensión a degenerar que la capa profunda. En concreto, por el perfil de expresión génica de cada célula, han i


 English
English